کلشی سین یک فرآورده طبیعی شگفت انگیز است که به دلیل دسترسی ساده، ساختمان نامتعارف و خصوصیات بیولوژیک قوی توجه بسیار زیادی را به خود جلب نموده است. شناخته ترین اثر این ترکیب، عملکرد ضد تکثیری آن به دلیل اتصال به پروتئینی به نام توبولین و جلوگیری از تشکیل دوک میتوزی است. به همین دلیل، به عنوان یک داروی بالقوه ضد تومور بخصوص برای درمان انواعی از تومورها که در برابر داروهای مرسوم ضد تومور مقاوم هستند، مطرح است. سمیت عمومی کلشیسین در مقادیر تجویزی بالا، نزدیک بودن دوزهای سمی و فارماکولوژیک و بهای پایین آن از عواملی است که منجر به دافعه و مقاومت صنعت داروسازی، به خصوص در درمان تومور، در استفاده از این آلکالوئید گیاهی منحصر به فرد است.
نام کلشی سین برگرفته از “کلچیس” منطقهای در نزدیکی دریای سیاه است که برای اولین بار گونه گیاهی کلشیکوم در آنجا پیدا شد. در پاپیروس ایبرز که قدیمیترین متن پزشکی است (با تاریخ بیش از 3500 سال) کلشی سین برای درمان درد و تورم توصیه شده است. دو دانشمند معروف ایرانی، محمد زکریای رازی (304 – 243 هجری شمسی) و ابوعلی سینا (416 – 359 هجری شمسی) برای اولین بار از کلشی سین در درمان بیماری نقرس استفاده کردند. کلشی سین در سال 1820 میلادی از منبع گیاهی خالص شد. در سال 1945 ساختمان شیمیایی آن، تعیین و در سال 1959 شکل صناعی آن ازیک مسیر شیمیایی بسیار طولانی تولید گردید. در سال 2009 میلادی سازمان غذا و داروی آمریکا کلشی سین را برای درمان نقرس و تب مدیترانه ای فامیلی تأیید نمود. امروزه در پزشکی، از کلشی سین در درمان نقرس حاد، تب مدیترانه ای فامیلی، اسکلرودرمای سیستمیک، آمیلوئیدوز و کندروکلسینوزیس استفاده می شود. بعلاوه، نتایج مطالعات متعدد حاکی از اثر مثبت آن در درمان انواعی از بیماریهای خودایمن، عفونت های مزمن، بیماریهای قلبی – عروقی، انواعی از آلرژی و بیماریهای تخریبی سیستم عصبی است (شکل 1).
ساختمان، عملکرد و مشتقات کلشی سین
کلشی سین یک نوع آلکالوئید تروپولونی است که در گیاهان جنس کلشیکوم، مرندرا و گلوریوزا به میزان قابل توجهی وجود دارد. ساختمان نامتعارف کلشی سین شامل سه حلقه هیدروکربنی 6، 7 و 7 وجهی چسبیده به هم است که در هسته مرکزی این سه حلقه جمعاً 12 اتم کربن وجود دارد. این سه حلقه به ترتیب با حروف A، B و C نامگذاری شده اند (شکل 1). کلشی سین از طریق حلقه های A و C به منطقه ای در حد فاصل شکل آزاد هترودیمر توبولین آلفا – بتا متصل می شود. در نتیجه این اتصال، هترودیمر توبولین نمی تواند به دنباله میکروتوبول در سلولهای یوکاریوتی اضافه شود. بدین جهت کلشی سین را به عنوان یک ترکیب تجزیه کننده (دپلیمره کننده) میکروتوبولها می شناسند. میکروتوبولها ریزلوله های توخالی حاصل از به هم پیوستن واحدهای هترودیمر توبولین آلفا – بتا هستند که در انواعی از فعالیتهای سلولی نقش تعیین کننده ای دارند. برای مثال، با تشکیل دوک، باعث جداسازی صحیح کروموزمها در اواخر تقسیم میتوز می شوند. بعلاوه، مسئول چیدن دقیق اندامکها در سیتوپلاسم و نگهداری شکل و موقعیت اجزای درون سلولی هستند و در رشد و مهاجرت سلول و انتقال مواد درون سلولی نقش مؤثری دارند. میکروتوبولها همچنین در بیان مولکولهای غشایی و تعامل سلول با زمینه خارج سلولی و سایر سلولهای اطراف اهمیت دارند. با توجه به اهمیت میکروتوبولها در انواعی از فعالیتهای درون و برون سلولی، توبولین هدف درمانی مهمی در انواعی از اختلالات پاتولوژیک و بیماریها است.
ترکیبات دارویی که توبولین را مورد هدف قرار می دهند، به دو دسته کلی تقسیم می شوند. دسته اول با تثبیت میکروتوبولها از جدا شدن زیرواحدهای توبولین (دپلیمریزاسیون تولوبولین) جلوگیری می کنند. ترکیبات دارویی خانواده “تاکسول” همچون پاکلیتاکسل یا دوستاکسل از این دسته هستند. در مقابل، دسته دوم شامل آلکالوئیدهای خانواده وینکا همچون وینکریستین یا وینبلاستین، با جلوگیری از به هم پیوستن زیرواحدهای توبولین (پلیمریزاسیون توبولین) اثر خود را اعمال می کنند. کلشی سین نیز ظاهراً شبیه به آلکالوئیدهای خانواده وینکا عمل می کند.
کلشی سین از محل حلقه های A و C به محلی در حد فاصل توبولین آلفا – بتا وصل می شود و بدین طریق از پیوستن زیرواحدهای بعدی به پلیمر توبولین ممانعت می کند. برخلاف اغلب داروهای خانواده تاکسول و وینکا، تعویض ایزوفرم توبولین بتا تاثیر محسوسی در اتصال کلشی سین به توبولین و اثر ضد تکثیری آن ندارد. تغییر ایزوفرم توبولین بخشی از مکانیسم مقاومت سلولهای توموری در برابر داروهای مختل کننده فعالیت دوک میتوزی است. شواهد حاکی از آن است که هرگونه دستکاری یا تغییر افزایشی یا کاهشی در ساختمان حلقه A کلشی سین، معمولاً اتصال آن به توبولین و خاصیت ضد میتوزی و ضد توموری آن را از بین می برد و به کاهش اثرات جانبی آن نیز کمکی نمی کند. بدین لحاظ این حلقه را مهمترین و حساسترین بخش در فعالیت کلشی سین می دانند. در مقابل، تغییرات جزئی در ساختمان حلقه های B و C معمولاً با از دست رفتن قابلیت اتصال کلشی سین به توبولین همراه نیست. گروههای متوکسی حلقه های A و C برای القای اثر سمی کلشی سین ضروری هستند، ولی تاثیری در واکنش آن با گلیکوپروتئین پی (P-gp) ندارند. در مقابل، وجود اتم نیتروژن در حلقه C در اتصال کلشی سین به P-gp نقش مهمی دارد. براین مبنا مطالعات متعددی در خصوص دستکاری حلقه C به هدف افزایش فعالیت، کاهش سمیت یا کاهش مقاومت دارویی کلشی سین انجام گرفته است. گلیکوپروتئین پی یک پروتئین غشایی پمپ کننده دارو به خارج سلول و بخشی از مکانیسم سلولهای توموری برای مقاومت علیه داروهای ضد تومور است.
آزمایشهای متعددی که برای تغییر در ساختمان کلشی سین انجام گرفته، عمدتاً به هدف کاهش سمیت عمومی و هدفمند نمودن اثر درمانی، افزایش فعالیت ضد توموری، کاهش عوارض، تغییر در حلالیت، رهایش و فراهمی زیستی آن بوده است. این تغییرات شامل دستکاری یا تعویض حلقه ها و استخلاف های اطراف حلقه ها، تولید اشکال پیش دارو، تولید اشکال هیبریدی، اشکال کونژوگه و تولید اشکال نانوذره و اشکال میسلی و لیپوزومی کلشی سین بوده است. نتایج بدست آمده حاکی از عدم موفقیت اغلب این مطالعات در دستیابی به اهداف مورد نظر بوده است. با این وجود، موارد معدودی از این مطالعات که نتایج قابل قبولی در مراحل اولیه (عمدتاً مطالعات برون تن) داشته اند، وارد مراحل آزمایش حیوانی یا کارآزمایی بالینی شده اند.
کلشی سین در درمان و یا کاهش عوارض ناشی از کووید – 19
با گذشت بیش از دو سال از شروع پاندمی کووید -19 شواهد بیانگر آن است که وقوع یک واکنش التهابی نابجا و ادامه دار، عامل اصلی آسیب بافت های درگیر همچون ریه و اختلال عملکرد در سایر اعضای بدن است. بعلاوه، این واکنش التهابی از دلایل عمده اختلال سیستم ایمنی و ناتوانی آن در حذف و پاکسازی ویروس و کنترل عوامل آسیب زا است. در کووید – 19 بار ویروس در افراد آلوده بی علامت و بیماران علامت دار مشابه است ولی شدت و مولفه های التهاب در این دو گروه تفاوت بسیار زیادی دارد. دلیل این تفاوت عمدتاً مربوط به مولفه های سیستم ایمنی ذاتی افراد مختلف است که پس از برخورد با ویروس پیامدهای متفاوتی به همراه دارد. برای مثال، نشان داده اند که در بیماران با علایم شدید، اتصال پروتئین شاخک ویروس کووید – 19 به انواع خاصی از دیمر گیرنده شبه نعل اسب (TLR) در سطح سلولهای پوششی مجاری تنفسی یا ماکروفاژها، به سلسه وقایعی در این سلولها منتهی می شود که نتیجه آن تولید مقدار بسیار کم اینترفرون های نوع یک، در قبال تولید زیاد انواعی از سایتوکاینها و کموکاینهای التهابی است.
آلوده شدن سلولهای پوششی مخاط تنفسی و ماکروفاژها با ویروس کووید – 19 و بیان پروتئینهای ویروس همچون پروتئین شاخک در سطح این سلولها، یا برخورد ماکروفاژهای سالم با سلولهای پوششی آلوده (از مسیر عرضه آنتی ژن یا تماس مستقیم)، به تولید انواعی از سایتوکاینها و کموکاینهای پیش التهابی منجر می شود. تشدید فراخوانی سلولهای التهابی همچون مونوسیتها و نوتروفیلها به واسطه سایتوکاینها و کموکاینهای آزاد شده و اختلال تدریجی در عملکرد سلولهای اندوتلیال عروق از عوامل تعیین کننده در توسعه التهاب و اختلال در عملکرد سیستم های هموستاز است که در ادامه به اختلال عملکرد سایر اعضای بدن و حتی مرگ بیمار منجر می شود. بر این اساس، می توان کووید – 19 را یک بیماری التهابی چند عضوی محسوب نمود که برای درمان و کاهش عوارض ناشی از آن، ضرورت تجویز ترکیبات ضد التهابی مناسب کاملاً روشن است. با این حال، بسیاری از متخصصین، تجویز ترکیبات ضد ویروس در کنار ترکیبات ضد التهابی را بخصوص در مراحل اولیه بیماری برای درمان ضروری می دانند.
با توجه به اثر ضد التهابی قوی کلشی سین و سابقه کاربرد آن در انواعی از بیمارهای التهابی، بخش عمده ای از محققین و متخصصین پزشکی، این ترکیب دارویی را به تنهایی یا همراه با ترکیبات دارویی دیگر برای درمان علایم و یا عوارض ناشی کووید – 19 از ابتدای این پاندمی مطرح کرده اند. شاهد این ادعا، ثبت 37 کارآزمایی بالینی تا ابتدای سال 2022 میلادی در سایت کارآزمایی بالینی امریکا است که در آنها از کلشی سین به تنهایی یا کلشی سین همراه داروهای دیگر برای درمان بیماری کووید – 19 پیشنهاد یا استفاده شده است. درمان بیماری کرونا با کلشی سین طبیعی همراه با مونوترپن های فنلی توسط شرکت زیست تولید رازی، از اولین مطالعات ثبت شده در سایت فوق است. حضور مونوترپن های فنلی در کنار کلشی سین در این پروتکل درمانی به هدف، الف- تکمیل اثر ضد التهابی کلشی سین و ب- افزودن اثرات ضد ویروسی و آنتی اکسیدان مونوترپن های فنلی است.
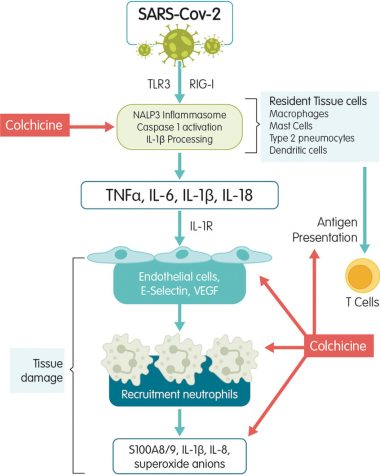
کلشی سین می تواند با اتصال به هترودیمر توبولین آلفا – بتا، از تشکل میکروتوبول ها در سلولهای التهابی جلوگیری نماید. نتیجه این کار، اختلال در الف- حرکت هدفمند (کموتاکسی)، ب- بیان مولکولهای چسبان همچون سلکتین E و سلکتین L، ج- انتقال درون سلولی مواد و د- فعالیت ترشحی (دگرانولاسیون) سلولهای التهابی است. از آنجا که غلظت کلشی سین در نوتروفیلها بسیار بیشتر (حداقل 50 برابر) از سایر سلول های التهابی است، به نظر می رسد این اثرات مهاری در نوتروفیلها قوی تر باشد. بخش دیگری از اثر ضد التهابی کلشی سین به دلیل مهار شکل گیری و فعالیت اینفلامازوم نوع NLRP3 است. اینفلامازوم NLRP3 یک ساختار بزرگ چند زیرواحدی در سیتوزول سلولهای ایمنی از جمله ماکروفاژها و مونوسیتها است که در فعال شدن آنزیم کاسپاز 1 و پردازش سایتوکاینهای پیش التهابی نقش مهمی دارد. ویروس کووید – 19 با فعال نمودن این نوع از اینفلامازوم به ویژه در مونوسیت ها، باعث افزایش شکل فعال کاسپاز 1 و اینترلوکین 18 (IL-18) می شود. نتیجه این فعالیت، افزایش تولید سایتوکاینهای التهابی از جمله اینترلوکین 6 (IL-6) اینترلوکین یک بتا (IL-1β) و فاکتور نکروز دهنده تومور آلفا (TNF-α) در بافت های درگیر است. اثر مهاری کلشی سین بر اینفلامازوم NLRP3 ضعیف تر از کورتیکواستروئیدها بخصوص دگزامتازون است. با این حال، عوارض منفی کورتیکواستروئیدها در سرکوب عمومی سیستم ایمنی و ناتوان نمودن آن در پاکسازی ویروس و یا عفونتهای ثانویه و تاثیر منفی آن بر عملکرد برخی اعضای بدن از جمله پانکراس، از دلایل ترجیحی کلشی سین نسبت به این داروها است. در کنار اثرات فوق، کلشی سین با مهار انواعی از فعالیت های التهابی نوتروفیلها، مونوسیتها و سلولهای اندوتلیال عروق از یک طرف و کاهش تحرک و فعالیت پلاکت ها از طرف دیگر، تعامل التهاب – ترومبوز را که یکی از مخاطرات بیماران در کووید – 19 است،کاهش می دهد.
کلید واژه: کلشی سین، التهاب، میکروتوبول، کووید – 19، اینفلامازوم
منابعی برای اطلاعات بیشتر
1- Gracheva IA, Shchegravina ES, Schmalz HG, et al. Colchicine alkaloids, and synthetic analogues: Current progress and perspectives. J. Med. Chem. 2022; in press.
DOI: 10.1021/acs.jmedchem.0c00222.
2 – Bonaventura A, Vecchié A, Dagna L, et al. Colchicine for COVID‑19: targeting NLRP3 inflammasome to blunt hyperinflammation. Inflamm. Res. 2022; 71:293–307.

